.png)

君实生物与礼来制药的新冠中和抗体联合疗法在降低病毒载量、减轻症状、降低新冠肺炎相关住院和急诊治疗方面均显示出良好疗效。
1月21日,礼来制药在《美国医学会杂志(JAMA)》发表了其发起的BLAZE-1临床试验研究结果。BLAZE-1是一项在美国49个中心进行的随机2/3期临床试验,旨在评估新冠病毒中和抗体的的疗效和安全性。结果显示,由礼来制药的Bamlanivimab(LY-CoV555)和君实生物的Etesevimab(JS016)组成的联合疗法显著降低了病毒载量,减轻了症状,且效果优于Bamlanivimab单药。

该联合疗法队列纳入了新近确诊为轻度至中度新冠肺炎的患者,并将其分配至联合治疗组(每种抗体各给药2800 mg)(n=112)或安慰剂组(n=156)。分析显示,联合疗法显著降低了第11天的病毒载量(p=0.01),达到了该研究的主要终点;同时,联合治疗达到了预设的临床终点,并显示耐受性良好,未报告药物相关的严重不良事件。
根据此前礼来制药的官方发布,礼来制药计划于2020年11月向FDA提交联合疗法的紧急使用授权(EUA)申请,预计最早在2021年第二季度之前取得数据并递交联合疗法的生物制品许可申请(BLA)。基于礼来制药的计划和临床疗效推测,由礼来制药和君实生物的新冠中和抗体组成的联合疗法有望在不久的将来获批紧急使用授权(EUA),君实生物有望从中受益。
全球中和抗体研发进展
面对新冠疫情,抗病毒药物一直是研究者和民众们关注的焦点。而在新冠特效药研发的赛道中,最受关注的就是中和抗体。
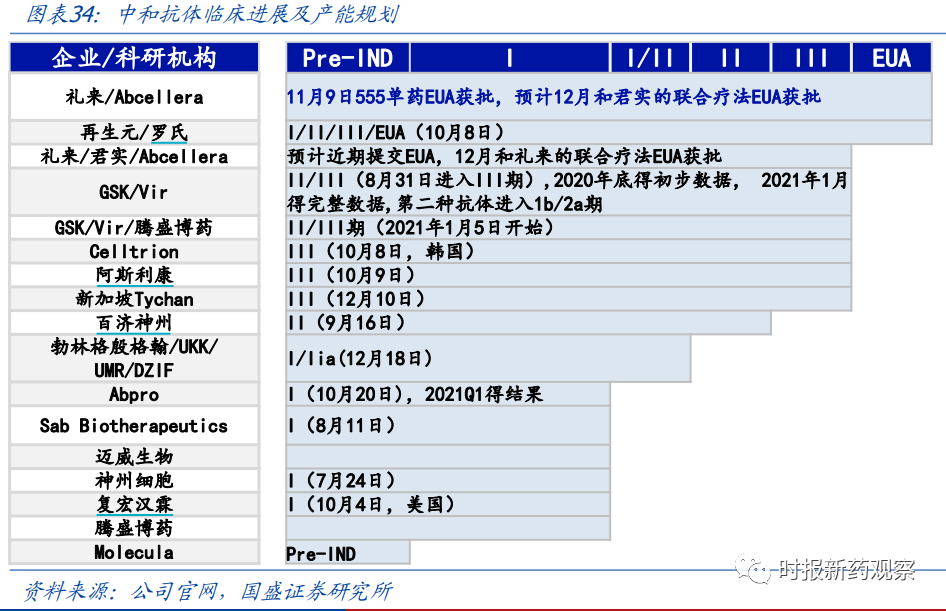
目前,海外制药巨头再生元与礼来处于研发的“第一梯队”,两家企业的新冠病毒中和抗体药物均获批紧急使用授权(EUA),研发进度进度靠前的还有葛兰素史克、Celltrion、阿斯利康等,均处于2/3期或3期临床阶段。
在国内,君实生物和中科院微生物所联合开发的JS016最早进入临床阶段,也是全球第二个进入临床试验阶段的中和抗体药物,研发进度处于全球领先水平。2020年5月,礼来与君实生物就JS016达成合作协议,君实生物持有大中华地区的所有权利,礼来负责大中华地区以外的临床开发、生产和商业化。据报道,盖茨基金会已经和礼来签订供药协议,其中就包括JS016。
此外,我国还有多家企业布局了此类药物。百济神州的新冠中和抗体目前处于2期临床,神州细胞、复宏汉霖、绿叶制药等的新冠中和抗体处于1期临床,1月20日,济民可信的新冠中和抗体在树兰(杭州)医院启动1期临床试验。
前景巨大但面临挑战
中和抗体是一种有抗病毒活性的单克隆抗体。凭借特异性和高亲和力特点,中和抗体能抢先与新冠病毒表面的刺突蛋白(S蛋白)受体结构域(RBD)结合,从而阻断病毒与宿主细胞结合,使病毒无法感染细胞,继而被免疫系统清除。
理论上,中和抗体兼具预防和治疗作用。在国金证券看来,相比疫苗,中和抗体具有三个优点。一是时间更快:短短几天到2周内,有效的中和抗体药物,即可让患者病毒负荷下降。而起到预防作用的疫苗,不仅需要观察安全性,还需要在注射完1针或2针或3针后,再观察更长时间。二是对症治疗:疫苗是给健康人群注射以期起到预防被感染的作用的,面对已经感染的患者或者需要短期防御的健康人,中和抗体是立竿见影的治疗手段。三是相对于各类创新型新冠疫苗,中和抗体的研发与生产制剂技术更为成熟。
目前全球新冠患者仍在持续增长,全球现有确诊患者超过2500万人,新冠肺炎的治疗用药极度缺乏,因此中和抗体用于新冠肺炎的治疗具有较好的前景。国金证券预计,新冠中和抗体上市后,有望达到10亿美元的重磅药量级。
不过,中和抗体的治疗作用也存在局限性。从目前披露的相关信息来看,中和抗体主要用于中轻症患者的治疗,此前,礼来和再生元的中和抗体重症患者临床试验均被叫停。君实生物CEO李宁曾表示,新冠疫苗和中和抗体所覆盖的人群并不完全一样,中和抗体主要是以治疗为主,以及面向对疫苗不反应的人群。
中和抗体还存在病毒变异的挑战。据CNBC网站1月13日报道,礼来制药首席执行官戴夫·里克斯表示,南非发现的变异株恐令该公司生产的一种抗体药物失效。中和抗体的趋势是采取联合疗法,联合疗法可以靶向不同的表位,能更大程度地抑制病毒。目前礼来的联合疗法和再生元的鸡尾酒疗法的共性是含有两个靶向新冠病毒S蛋白RBD不同结合位点的抗体,当体内有靶向两个不同结合位点的抗体存在时,病毒需要在多个遗传位点产生变异才能成功逃逸,由此可以大大降低耐药率。
此外,目前中和抗体销售也低于预期。据报道,中和抗体品种在美国上市后实际利用率相对较低,目前已分发出去的中和抗体产品仅5%-20%被使用。专家分析导致这个情况的原因有多种,如中和抗体使用便捷性较差,需要到有专业医疗资质的地点进行静脉注射;中和抗体仅批准用于治疗轻症患者,大部分患者会等到病情较为严重的时候才选择就医,因此错过了使用中和抗体治疗的黄金窗口期。
声明:证券时报力求信息真实、准确,文章提及内容仅供参考,不构成实质性投资建议,据此操作风险自担。

.gif) 证券时报APP
证券时报APP
.gif) 微信公众号
微信公众号